Colite ulcerosa. Aifa approva rimborsabilità di mirikizumab, primo di una nuova classe terapeutica
L’Agenzia Italiana del Farmaco ha approvato la rimborsabilità del primo antagonista dell’interleuchina-23p19 (IL-23p19), mirikizumab, per il trattamento della colite ulcerosa (UC) attiva da moderata a grave nei pazienti adulti.
Mirikizumab è l’unico farmaco attualmente rimborsato in Italia per la UC a colpire selettivamente la subunità p19 di IL-23, che svolge un ruolo cruciale nell’infiammazione correlata alla UC. Un meccanismo di azione che permette di offrire sollievo da sintomi chiave quali frequenza evacuativa, sanguinamento rettale e urgenza intestinale, indipendentemente dall’uso precedente di farmaci biologici.
Il programma di studi clinici Lucent, su cui si è basata l’approvazione del farmaco, dimostra l’efficacia in adulti con malattia da moderata a grave: dopo 12 settimane di trattamento, quasi due terzi hanno raggiunto la risposta clinica e quasi un quarto ha raggiunto la remissione clinica.
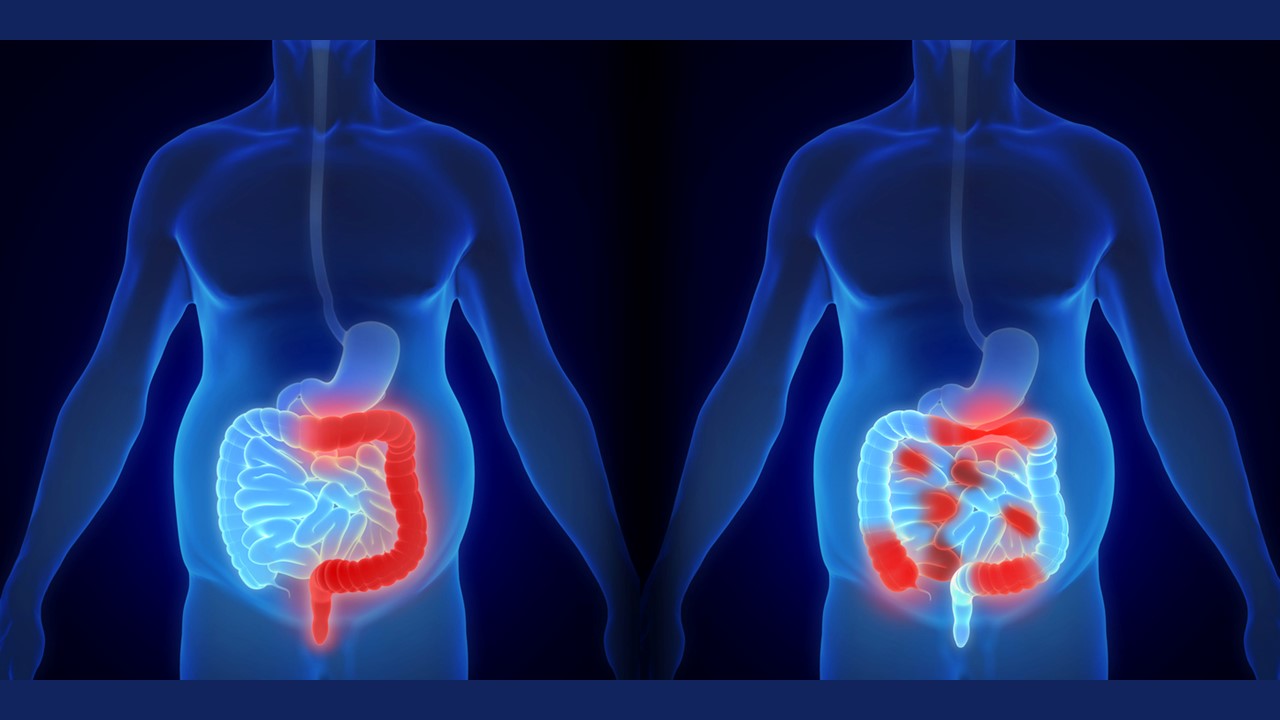
La UC è una condizione infiammatoria che in Italia si stima colpisca circa 150.000 persone, con oltre 4000 nuove diagnosi all’anno, prevalentemente in persone giovani.
Per le persone che vivono con UC i sintomi che hanno un maggior impatto sono la diarrea, l’urgenza intestinale e gli incidenti correlati all’urgenza intestinale. L’urgenza intestinale ed eventuali incidenti a essa correlati rappresentano le ragioni principali per cui le persone evitano di avere vita sociale.